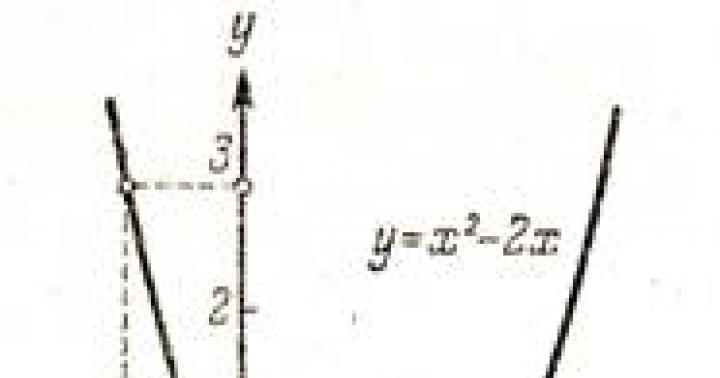(мон(о)оксид азота , окись азота , нитрозил-радикал ) NO - несолеобразующий оксид азота . В нормальных условиях он представляет собой бесцветный газ, плохо растворимый в воде. Сжижается с трудом; в жидком и твёрдом виде имеет голубой цвет.
Наличие неспаренного электрона обусловливает склонность NO к образованию слабосвязанных димеров N 2 O 2 . Это непрочные соединения с ΔH ° димеризации около 17 кДж/моль. Жидкий оксид азота(II) на 25 % состоит из молекул N 2 O 2 , а твёрдый оксид целиком состоит из них.
Получение
Оксид азота(II) - единственный из оксидов азота, который можно получить непосредственно из свободных элементов соединением азота с кислородом при высоких температурах (1200-1300 °C) или в электрическом разряде. В природе он образуется в атмосфере при грозовых разрядах (тепловой эффект реакции −180,9 кДж):
При понижении температуры оксид азота(II) разлагается на азот и кислород, но если температура падает резко, то не успевший разложиться оксид существует достаточно долго: при низкой температуре скорость распада невелика. Такое резкое охлаждение называется «закалкой» и используется при одном из способов получения азотной кислоты .
В лаборатории его обычно получают взаимодействием 30%-ной HNO 3 с некоторыми металлами , например, с медью :
Более чистый, не загрязнённый примесями NO можно получить по реакциям:
Промышленный способ основан на окислении аммиака при высокой температуре и давлении при участии , Cr 2 O 3 (как катализаторов):
Химические свойства
При комнатной температуре и атмосферном давлении происходит окисление NO кислородом воздуха:
Для NO характерны также реакции присоединения галогенов с образованием нитрозилгалогенидов, в этой реакции NO проявляет свойства восстановителя с образованием нитрозилхлорида :
В присутствии более сильных восстановителей NO проявляет окислительные свойства:
В воде NO мало растворим и с ней не реагирует, являясь несолеобразующим оксидом.
Физиологическое действие
Как и все оксиды азота (кроме N 2 O), NO - токсичен, при вдыхании поражает дыхательные пути.
За два последних десятилетия было установлено, что эта молекула NO обладает широким спектром биологического действия, которое условно можно разделить на регуляторное, защитное и вредное. NO действует как посредник в передаче клеточных сигналов внутри клетки и между клетками. Оксид азота, производимый клетками эндотелия сосудов, отвечает за расслабление гладких мышц сосудов и их расширение (вазодилатацию), предотвращает агрегацию тромбоцитов и адгезию нейрофилов к эндотелию, участвует в различных процессах в нервной, репродуктивной и иммунной системах. NO также обладает цитотоксическими и цитостатическими свойствами. Клетки-киллеры иммунной системы используют оксид азота для уничтожения бактерий и клеток злокачественных опухолей. С нарушением биосинтеза и метаболизма NO связаны такие заболевания, как эссенциальная артериальная гипертензия, ишемическая болезнь сердца, инфаркт миокарда, первичная легочная гипертензия, бронхиальная астма, невротическая депрессия, эпилепсия, нейродегенеративные заболевания (болезнь Альцгеймера, болезнь Паркинсона), сахарный диабет , импотенция и др.
Оксид азота может синтезироваться несколькими путями. Растения используют неферментативную фотохимическую реакцию между NO 2 и каротиноидами. У животных синтез осуществляют семейство NO-синтаз (NOS). NOS-ферменты - члены гем-содержащего суперсемейства ферментов, названных монооксигеназами. В зависимости от структуры и функций, NOS могут быть разделены на три группы: эндотелиальные (eNOS), нейрональные (nNOS) и индуцибельные (iNOS). В активный центр любой из NO-синтаз входит железопорфириновый комплекс, содержащий аксиально координированный цистеин или метионин. Хотя все изоформы NOS катализируют образование NO, они являются продуктами различных генов, каждая из них имеет свои особенности как в механизмах действия и локализации, так и в биологическом значении для организма. Поэтому указанные изоформы принято также подразделять на конститутивную (cNOS) и индуцибельную (iNOS) синтазы оксида азота.
cNOS постоянно находится в цитоплазме, зависит от концентрации ионов кальция и кальмодулина (белок, являющийся внутриклеточным посредником переноса ионов кальция) и способствует выделению небольшого количества NO на короткий период в ответ на стимуляцию рецепторов. Индуцибельная NOS появляется в клетках только после индукции их бактериальными эндотоксинами и некоторыми медиаторами воспаления, такими как гамма-интерферон, фактор некроза опухоли и др. Количество NO, образующегося под влиянием iNOS, может варьировать и достигать больших количеств (наномолей). При этом продукция NO сохраняется длительнее.
Характерной особенностью NO является способность быстро (менее чем за 5 секунд) диффундировать через мембрану синтезировавшей его клетки в межклеточное пространство и легко (без участия рецепторов) проникать в клетки-мишени. Внутри клетки он активирует одни и ингибирует другие ферменты, участвуя в регуляции клеточных функций и фактически действуя как локальная сигнальная молекула. NO играет ключевую роль в подавлении активности бактериальных и опухолевых клеток путем либо блокирования некоторых их железосодержащих ферментов, либо путем повреждения их клеточных структур оксидом азота или свободными радикалами, образующимися из оксида азота. Одновременно в очаге воспаления накапливается супероксид, который вызывает повреждение белков и липидов клеточных мембран, что и объясняет его цитотоксическое действие на клетку-мишень. Следовательно, NO, избыточно накапливаясь в клетке, может действовать двояко: с одной стороны вызывать повреждение ДНК и с другой - давать провоспалительный эффект.
Оксид азота способен инициировать образование кровеносных сосудов . В случае инфаркта миокарда оксид азота играет положительную роль, так как индуцирует новый сосудистый рост, но при раковых заболеваниях тот же самый процесс вызывает развитие опухолей, способствуя питанию и росту раковых клеток. С другой стороны, вследствие этого улучшается доставка оксида азота в опухолевые клетки. Повреждение ДНК под действием NO является одной из причин развития апоптоза (запрограммированный процесс клеточного «самоубийства», направленный на удаление клеток, утративших свои функции). В экспериментах наблюдалось дезаминирование дезоксинуклеозидов, дезоксинуклеотидов и неповрежденной ДНК при воздействии раствора, насыщенного NO. Этот процесс ответствен за повышение чувствительности клеток к алкилирующим агентам и ионизирующему излучению, что используется в антираковой терапии.
Клиренс NO (скорость очищения крови от NO в процессе его химических превращений) происходит путем образования нитритов и нитратов и составляет в среднем не более 5 секунд. В клиренс могут быть вовлечены промежуточные ступени, связанные со взаимодействием с супероксидом или с гемоглобином с образованием пероксинитрита . Оксид азота может быть восстановлен NO-редуктазой - ферментом, тесно связанным с NO-синтазой.
Применение
Получение NO является одной из стадий получения азотной кислоты .
См. также
| Оксиды азота | |||||
 Оксид азота(I) (N 2 O) Оксид азота(I) (N 2 O)
|
 Оксид азота(II) (NO) Оксид азота(II) (NO)
|
||||
 Оксид азота(III) (N 2 O 3) Оксид азота(III) (N 2 O 3)
|
 | ||||
При обычной температуре N 2 O - бесцветный газ со слабым приятным запахом и сладковатым вкусом; обладает наркотическим действием, вызывая сначала судорожный смех, затем - потерю сознания.
Способы получения
1. Разложение нитрата аммония при небольшом нагревании:
NH 4 NO 3 = N 2 O + 2Н 2 О
2. Действие HNO 3 на активные металлы
10HNO 3 (конц.) + 4Са = N 2 O + 4Ca(NO 3) 2 + 5Н 2 О
Химические свойства
N 2 O не проявляет ни кислотных, ни основных свойств, т. е. не взаимодействует с основаниями, с кислотами, с водой (несолеобразующий оксид).
При Т > 500"С разлагается на простые вещества. N 2 O - очень сильный окислитель. Например, способен в водном растворе окислить диоксид серы до серной кислоты:
N 2 O + SO 2 + Н 2 О = N 2 + H 2 SO 4
NO - оксид азота (II), монооксид азота.
При обычной температуре NO - бесцветный газ без запаха, малорастворимый в воде, очень токсичный (в больших концентрациях изменяет структуру гемоглобина).
Способы получения
1. Прямой синтез из простых веществ может быть осуществлен только при очень высокой Т:
N 2 + O 2 = 2NО - Q
2. Получение в промышленности (1-я стадия производства HNO 3).
4NH 3 + 5O 2 = 4NО + 6Н 2 О
3. Лабораторный способ - действие разб. HNO 3 на тяжелые металлы:
8HNO 3 + 3Cu = 2NO + 3Cu(NO 3) 2 + 4Н 2 О
Химические свойства
NO - несолеобразующий оксид (подобно N 2 О). Обладает окислительно-восстановительной двойственностью.
I. NO - окислитель
2NO + SO 2 + Н 2 О = N 2 O + H 2 SO 4
2NO + 2H 2 = N 2 + 2Н 2 О (со взрывом)
II. NO - восстановитель
2NO + O 2 = 2NO 2
10NO + 6KMnO 4 + 9H 2 SO 4 = 10HNO 3 + 3K 2 SO 4 + 6MnSO 4 + 4Н 2 О
NO 2 - оксид азота (IV), диоксид азота
При обычной температуре NO 2 - красно-бурый ядовитый газ с резким запахом. Представляет собой смесь NO 2 и его димера N 2 O 4 в соотношении -1:4. Диоксид азота хорошо растворяется в воде.
Способы получения
I. Промышленный - окисление NO: 2NO + O 2 = 2NO 2
II. Лабораторные:
действие конц. HNO 3 на тяжелые металлы: 4HNO 3 + Сu = 2NO 2 + Cu(NO 3) 2 + 2Н 2 О
разложение нитратов: 2Pb(NO 3) 2 = 4NO 2 + O 2 + 2РbО
Химические свойства
NO 2 - кислотный оксид, смешанный ангидрид 2-х кислот
NO 2 взаимодействует с водой, основными оксидами и щелочами. Но реакции протекают не так, как с обычными оксидами - они всегда окислительно - восстановительные. Объясняется это тем, что не существует кислоты со С.О. (N) = +4, поэтому NO 2 при растворении в воде диспропорционирует с образованием 2-х кислот - азотной и азотистой:
2NO 2 + Н 2 О = HNO 3 + HNO 2
Если растворение происходит в присутствии O 2 , то образуется одна кислота - азотная:
4NO 2 + 2Н 2 О + O 2 = 4HNO 3
Аналогичным образом происходит взаимодействие NO 2 со щелочами:
в отсутствие O 2: 2NO 2 + 2NaOH = NaNO 3 + NaNO 2 + Н 2 О
в присутствии O 2: 4NO 2 + 4NaOH + O 2 = 4NaNO 3 + 2Н 2 О
NO 2 - очень сильный окислитель
По окислительной способности NO 2 превосходит азотную кислоту. В его атмосфере горят С, S, Р, металлы и некоторые органические вещества. При этом NO 2 восстанавливается до свободного азота:
10NO 2 + 8P = 5N 2 + 4P 2 O 5
2NO 2 + 8HI = N 2 + 4I 2 + 4Н 2 О (возникает фиолетовое пламя)
В присутствии Pt или Ni диоксид азота восстанавливается водородом до аммиака:
2NO 2 + 7Н 2 = 2NH 3 + 4Н 2 О
Как окислитель NO 2 используется в ракетных топливах. При его взаимодействии с гидразином и его производными выделяется большое количество энергии:
2NO 2 + 2N 2 H 4 = 3N 2 + 4Н 2 О + Q
N 2 O 3 и N 2 O 5 - неустойчивые вещества
Оба оксида имеют ярко выраженный кислотный характер, являются соответственно ангидридами азотистой и азотной кислот.
N 2 O 3 как индивидуальное вещество существует только в твердом состоянии ниже Т пл. (-10 0 С).
С повышением температуры разлагается: N 2 O 3 → NO + NO 2
N 2 O 5 при комнатной температуре и особенно на свету разлагается так энергично, что иногда самопроизвольно взрывается.
Эта статья описывает оксиды азота как химические соединения; об образовании и способах сокращения выбросов оксидов азота при горении см. NOx (оксиды азота) .
Окси́ды азо́та - неорганические бинарные соединения азота с кислородом .
Энциклопедичный YouTube
1 / 3
Опыты по химии. Получение оксида азота (II); окисление его кислородом
Закись азота
О пользе оксида азота в организме. Найтворкс
Субтитры
Список оксидов
Известны 10 соединений азота с кислородом. Кроме пяти классических оксидов азота - закиси азота N 2 O, окиси азота NO, оксида азота(III) N 2 O 3 , диоксида азота NO 2 и оксида азота(V) N 2 O 5 - известны также димер диоксида азота N 2 O 4 и 4 малостабильных соединения: нитрозилазид NON 3 , нитрилазид NO 2 N 3 , тринитрамид N(NO 2) 3 и нитратный радикал NO 3 .
N 2 O
Несолеобразующий оксид. При нагревании разлагается на азот и кислород . При высоких концентрациях N 2 O возбуждает нервную систему («веселящий газ »). В медицине N 2 O применяют как слабое средство для наркоза , токсичен. Также N 2 O называют закисью азота. Закись азота иногда используется для улучшения технических характеристик двигателей внутреннего сгорания. В случае автомобильных применений вещество, содержащее закись азота, и горючее впрыскиваются во впускной (всасывающий) коллектор двигателя, что приводит к следующим результатам:
- снижает температуру всасываемого в двигатель воздуха, обеспечивая плотный поступающий заряд смеси;
- увеличивает содержание кислорода в поступающем заряде;
- повышает скорость (интенсивность) сгорания в цилиндрах двигателя.
NO
Оксид азота NO (монооксид азота ) - бесцветный газ, незначительно растворим в воде. Не взаимодействует с водой, растворами кислот и щелочей. Оксид азота(II) - очень реакционное соединение, может вступать в реакции присоединения с рядом солей (нитрозосоли), с галогенами (напр., нитрозилхлорид NOCl), органическими соединениями. При обычной температуре NO соединяется с кислородом с образованием NO 2 . Оксид NO получают каталитическим окислением аммиака при производстве азотной кислоты .
N 2 O 3 (III)
Оксид N 2 O 3 (триоксид диазота, азотистый ангидрид ) - темно-синяя жидкость, неустойчивая при обычных условиях, взаимодействует с водой, образуя азотистую кислоту HNO 2 .
NO 2 (IV)
Оксид азота NO 2 (диоксид азота ) - бурый газ, токсичен, тяжелее воздуха, легко сжижается. При комнатной температуре NO 2 находится в смеси с его бесцветным димером N 2 O 4 , приблизительно 1:1. Взаимодействует с водой:
2 N O 2 + H 2 O → H N O 3 + H N O 2 {\displaystyle {\mathsf {2NO_{2}+H_{2}O\rightarrow HNO_{3}+HNO_{2}}}}и растворами щелочей:
2 N O 2 + 2 N a O H → N a N O 3 + N a N O 2 + H 2 O {\displaystyle {\mathsf {2NO_{2}+2NaOH\rightarrow NaNO_{3}+NaNO_{2}+H_{2}O}}}Сильный окислитель. Многие вещества (
Оксиды и гидроксиды азотаТАЙНА СТЕПЕНЕЙ ОКИСЛЕНИЯ
Азот образует ряд оксидов, формально отвечающих всем возможным степеням окисления от +1 до +5: N 2 O, NО, N 2 O 3 , NO 2 , N 2 O 5 , однако всего два из них - оксид азота(II) и оксид азота(IV) - не только устойчивы при обычных условиях, но и активно задействованы в природном и промышленном круговоротах азота. Поэтому мы займемся изучением именно их свойств (в сравнении). Начнем, как обычно, со строения молекул.
Cтроение молекул оксидов азота
Молекула
NO. Строение предположить
достаточно просто: у кислорода два неспаренных
электрона, у азота три – образуется двойная
связь и один неспаренный электрон в остатке...
Непросто ответить на вопрос, почему такая
«нестандартная» молекула устойчива. Кстати,
стоит заметить, что устойчивые свободные
радикалы – молекулы с неспаренными электронами
– в природе достаточно редки. Можно
предположить, что молекулы NO будут спариваться и
образовывать удвоенную, или димерную, молекулу
ONNO. Таким образом удается решить проблему
неспаренного электрона.
Молекула
NO 2 . Казалось бы, чего проще –
к молекуле NО по неспаренному электрону
присоединился атом кислорода. (На самом деле
присоединяется не атом, а молекула, и не к NО, а к
димеру ОNNO. Поэтому-то и уменьшается скорость
присоединения с повышением температуры – димер
разваливается на половинки.) И теперь уже у
кислорода появился неспаренный электрон –
молекула оксида азота(IV) тоже свободный радикал.
Однако известно, что при соединении двух молекул
NО 2 и образовании молекулы N 2 O 4
связь осуществляется через атомы азота, значит,
именно у азота и должен бы быть этот самый
неспаренный электрон. Как это можно осуществить?
Ответ нетрадиционен, но вполне в «характере»
азота – донорно-акцепторная связь. Используя
логику, рассмотрим электроны, которые есть у
атома азота в молекуле NО. Это неспаренный
электрон, свободная пара электронов и еще два
электрона на связи с кислородом – всего пять. А у
атома кислорода, «выходящего на связь», шесть
электронов на четырех орбиталях. Если
расположить их по два, то одна орбиталь останется
свободной. Вот именно ее и занимает пара
электронов атома азота, а неспаренный электрон в
этой связи оказывается совершенно ни при чем
(рис. 1, 2).
Стоит упомянуть еще один момент – раз пара
электронов, находящаяся на s
-орбитали,
«пошла на связь», она была просто обязана
подвергнуться гибридизации – очень сложно
предложить второму атому в общее пользование
пару электронов, равномерно распределенную по
поверхности первого атома. Возникает вопрос:
какой тип гибридизации использует атом? Ответ:
три электронные орбитали азота находятся в
состоянии sp 2
-гибридизации. Молекула NO 2
угловая, угол 134° (угол больше 120° потому, что один
электрон отталкивает от себя электроны связи
слабее, чем пара электронов) (рис. 3–5).
Физические свойства оксидов азота
Оксид азота(II) NO. Кристаллическая решетка молекулярная; молекула легкая, слабополярная (электроотрицательность кислорода выше, чем у азота, но не намного). Можно предположить, что температуры плавления и кипения будут низкими, но выше, чем у азота, т. к. какая-никакая полярность молекулы дает возможность подключать электростатические силы притяжения к просто межмолекулярным силам. Образование димера тоже способствует повышению температуры кипения, утяжеляя молекулу. Строение молекулы позволяет предположить и невысокую растворимость в воде – растворителе заметно более полярном, чем NO. Отдельно стоит подчеркнуть, что оксид азота(II) не имеет ни цвета, ни запаха.
Оксид азота(IV)
NO 2 .
Кристаллическая решетка тоже молекулярная,
однако поскольку сама молекула тяжелее NO и
склонность к димеризации у нее заметно выше, то
плавиться и кипеть это вещество должно при
заметно более высоких температурах. Температура
кипения составляет 21 °С, поэтому при обычных
условиях – 20 °С и 760 мм рт. ст. – оксид азота(IV)
жидкий.
Теперь займемся растворимостью. Вспомним, что
под словом «растворимость» могут
подразумеваться и химические реакции с водой;
главное, чтобы растворитель поглотил
растворяемое. При реакции оксидов с водой, как
известно, получаются гидроксиды – формально это
просто гидратированные оксиды, но реальность
зачастую преподносит массу интересного и совсем
неформального. Вот и этот оксид азота в воде
растворяется, одновременно с ней реагируя, и
получается при этом сразу две кислоты!
Отметим, что оксид азота(IV) имеет и
характерный резкий запах, и рыжевато-бурый цвет,
оттенки которого отличаются друг от друга в
зависимости от концентрации. Именно за этот цвет
выбросы оксидов азота в атмосферу называют
«лисьими хвостами».
Вы спросите: а где же тайна? Первая часть тайны
степеней окисления перед вами: почему у элемента
пятой (нечетной) группы устойчивы оксиды с
четными степенями окисления? (При этом еще и
свободные радикалы!) В наиболее общем смысле
ответ очевиден – раз устойчивы, значит, им так
выгодно. Энергетически. А почему? Видимо, дело в
специфике строения атомов азота и кислорода – у
них слишком много электронов и слишком мало
орбиталей. Именно «орбитальные возможности»
диктуют свои правила, устанавливают такие
«энергетические выгоды». Тогда цифры «два» и
«четыре» становятся понятными: двух электронов
не хватает кислороду до восьми и у обоих атомов
только по четыре орбитали.
А еще можно сказать, что NO просто... ждет молекулу
кислорода, чтобы превратиться в NО 2 .
Используя метафору, отметим, что «смысл жизни»
многих атомов – стремление найти себе «партнера
по жизни» – атом или атомы другого элемента. Хотя
есть, конечно, и «убежденные холостяки» типа
золота.
Химические свойства оксидов азота
1. Реакции с металлами. Поскольку атом азота в положительных степенях окисления является окислителем, причем чем выше степень окисления, тем сильнее способность отбирать электроны у других атомов, то с металлами – по сути своей восстановителями – оксиды азота будут реагировать. Продукты при этом могут получаться совсем разные, в зависимости от условий реакции и самого металла. Например, раскаленной меди все оксиды азота отдают кислород, а сами превращаются в простое вещество азот:

По количеству образовавшихся оксида меди и азота можно установить, какой именно из оксидов азота реагировал с медью.
2. Реакции с неметаллами.
В первую
очередь рассмотрим реакции с кислородом. Здесь
между оксидами наблюдается различие, и весьма
существенное.
Оксид
NO реагирует с кислородом с
образованием оксида азота(IV). Реакция обратимая.
Причем с повышением температуры скорость этой
реакции уменьшается:
2NO + O 2 = 2NO 2 .
Оксид
NO 2 с кислородом вообще не
реагирует.
Озон переводит оба оксида в оксид азота(V).
Оксид азота(II)
NO присоединяет озон
полностью:
2NO + O 3 = N 2 O 5 .
Оксид азота(IV) NO 2 в реакции с озоном выделяет еще и кислород:
2NO 2 + O 3 = N 2 O 5 + O 2 .
3. Реакции с водой . Оксид NO с водой не реагирует. Оксид NO 2 с водой образует две кислоты – азотную (степень окисления азота +5) и азотистую (степень окисления азота +3). В присутствии кислорода оксид NO 2 целиком переходит в азотную кислоту:
2NO 2 + Н 2 O = НNО 3 + НNO 2 ,
4NO 2 + O 2 + 2Н 2 О = 4НNО 3 .
4. Реакции c кислотами.
Ни один из
оксидов – NO или NO 2 – не реагирует с
кислотами.
5. Реакции со щелочами
. Оба оксида азота
реагируют со щелочами.
Оксид NO образует с щелочью соль азотистой кислоты, оксид азота(I) и азот:
10NO + 6NaOH = 6NaNO 2 + N 2 O + N 2 + 3H 2 O.
Оксид NO 2 образует с щелочью соли двух кислот – азотной и азотистой:
2NO 2 + 2NaOH = NaNO 3 + NaNO 2 + H 2 O.
Вернемся к нашей тайне степеней окисления. При
переходе кислородных соединений азота из
состояния «газ», где свободно можно двигаться, в
состояние «водный раствор», где больше толкотни,
где процветает коллективизм, где существуют и
активно действуют полярные молекулы воды, никто
уже не позволит молекуле, атому или иону быть в
одиночестве, происходит «смена ориентации».
Устойчивыми становятся как раз нечетные степени
окисления, как и положено элементу из нечетной
группы. (Устойчивыми, правда, относительно.
Азотистая кислота, например, может существовать
только в растворе, иначе она разлагается. Но
кислот, формально соответствующих оксидам
азота(II) и (IV), вообще не существует. Все познается
в сравнении.)
Интересно, что со щелочами реагирует не только
явно кислотный оксид NO 2 , но и NО – по
свойствам и степени окисления некислотный, при
этом получаются соединения других степеней
окисления – нечетных! Тайна? Вполне!
Строение молекулы гидроксида азота(V) – азотной кислоты
Из гидроксидов азота мы рассмотрим один, но
наиболее многотоннажный – азотную кислоту.
Молекула азотной кислоты полярна (в первую
очередь из-за разной электроотрицательности
кислорода и водорода, потому что азот как бы
скрыт внутри молекулы) и асимметрична. Все три
имеющихся в ней угла между связями азота с
кислородом разные. Формальная степень окисления
азота высшая, т. е. +5. Но при этом только четыре
связи у атома азота с другими атомами –
валентность азота равна четырем. Еще одна тайна.
Понятно, как может получиться так, что
валентность атома
численно больше его
степени окисления
. Для этого достаточно
образовать в молекуле связь между одинаковыми
атомами. Например, в пероксиде водорода у
кислорода валентность два, а степень окисления
только –1. Общую электронную пару связи с
водородом кислороду удалось подтянуть к себе
поближе, а пара связи двух атомов кислорода так и
находится строго посередине. Но как сделать так,
чтобы валентность атома
была меньше
степени окисления
?
Давайте подумаем: а как вообще устроена молекула
азотной кислоты? Строение молекулы легче понять,
если рассмотреть процесс ее получения. Азотная
кислота получается при реакции оксида азота(IV) с
водой (в присутствии кислорода): две молекулы NO 2
одновременно «атакуют» молекулу воды своими
неспаренными электронами, в результате связь
водорода с кислородом разрывается не как обычно
(пара электронов у кислорода и «голый протон»), а
«по-честному» – одной молекуле NO 2
достается водород со своим электроном, другой –
радикал ОН (рис. 6). Образуются две кислоты: обе
кислоты сильные, обе быстро отдают свой протон
ближайшим молекулам воды и остаются в итоге в
виде ионов и . Ион нестоек, две молекулы НNО 2
разлагаются на воду, NО 2 и NО. Оксид NO
реагирует с кислородом, превращаясь в NО 2 , и
так до тех пор, пока не получится одна только
азотная кислота.
Формально выходит, что с одним атомом
кислорода атом азота связан двойной связью, а с
другим – обычной одинарной связью (этот атом
кислорода связан еще и с атомом водорода). С
третьим атомом кислорода азот в HNO 3 связан
донорно-акцепторной связью, причем в качестве
донора выступает атом азота. Гибридизация атома
азота при этом должна быть sр 2
из-за
наличия двойной связи, что определяет структуру
– плоский треугольник. Реально получается, что
действительно фрагмент из атома азота и трех
атомов кислорода – плоский треугольник, только в
молекуле азотной кислоты этот треугольник
неправильный – все три угла ОNО разные,
следовательно, и разные стороны треугольника.
Когда же молекула диссоциирует, треугольник
становится правильным, равносторонним. Значит, и
атомы кислорода в нем становятся равноценными!
Одинаковыми становятся и все связи (двойная
связь короче одинарной). Каким образом?
Давайте рассуждать. sр 2
-Гибридизация
атома азота принуждает к такому же типу
гибридизации и атомы кислорода. Получается
плоская структура, поперек которой расположены
не участвующие в гибридизации р-орбитали,
имеющиеся у всех четырех атомов.
Теперь разберемся с общим количеством валентных
электронов: ион
содержит пять электронов азота, по шесть у трех
атомов кислорода и еще один, придающий заряд иону
в целом, итого двадцать четыре. Из них шесть
электронов требуется для образования трех
одинарных связей, двенадцать электронов
расположены по периметру молекулы на гибридных
орбиталях (по две электронные пары у каждого
атома кислорода), остается шесть электронов на
четыре те самые р
-орбитали, не участвующие в
гибридизации. Единственное возможное в данном
случае разумное объяснение – это обобществление
всеми атомами своих электронов в единое
электронное облако (рис. 7). Этому способствуют
малые радиусы атомов и малые межатомные
расстояния. А симметрия обычно энергетически
выгодна и поэтому повышает устойчивость
конструкции в целом. Это не единственный случай
обобществления электронов несколькими атомами,
похожее «коллективное электронное хозяйство»
встречается в органической химии, например в
ароматических соединениях.
Вернемся, однако, к предсказаниям свойств азотной кислоты, исходя из представлений о структуре молекулы. Очевидная выгодность пребывания в виде иона объясняет не только высокую степень диссоциации кислоты в водном растворе, но и возможность диссоциации безводной кислоты. И именно диссоциация определяет физические свойства этого вещества.
Физические свойства азотной кислоты
Соединение ионизированное, пусть даже и
частично, сложно перевести в газ. Таким образом,
температура кипения должна бы быть достаточно
высокой, однако при такой небольшой молекулярной
массе (и из-за высокой подвижности) температура
плавления высокой быть не должна. Следовательно,
агрегатное состояние при 20 °С – жидкое.
Что касается растворимости в воде, то, как и
многие другие полярные жидкости, азотная кислота
легко смешивается с водой в любых соотношениях.
Чистая азотная кислота бесцветна и не имеет
запаха. Однако из-за разложения на кислород и
оксид азота(IV), который в ней же и растворяется,
можно сказать, что обычная концентрированная
азотная кислота имеет желтобурый цвет и
характерный для NO 2 резкий запах.
Посмотрим, как влияет строение молекулы азотной
кислоты на ее химические свойства.
Химические свойства азотной кислоты
Главное, что мы должны отметить, – наличие
высшей степени окисления атома азота
ограничивает свойства азотной кислоты, с
окислителями она не реагирует. Зато с
восстановителями, в первую очередь с металлами,
она реагирует нетрадиционно и разнообразно.
1. Реакции с металлами
. С металлами
азотная кислота реагирует как сильный
окислитель даже в разбавленных растворах (в
отличие от серной кислоты, проявляющей свои
окислительные свойства только в
концентрированном виде). Образуется обычно
нитрат металла, но вместо водорода выделяются
газообразные соединения азота: NО 2 , NО, N 2 O,
N 2 или аммиак, который в кислой среде сразу
переходит в ион аммония. В принципе при реакции
металла с азотной кислотой образуется весь этот
«букет» газов, но в зависимости от металла и
концентрации кислоты те или иные компоненты
будут превалировать.
Так, в лабораторных условиях оксид азота(II)
обычно получают при взаимодействии медных
стружек с азотной кислотой плотностью 1,2 г/см 3 ,
т. е. при обработке меди разбавленной кислотой в
газообразных продуктах реакции явно превалирует
именно этот оксид:
А вот при реакции азотной кислоты той же плотности (а следовательно, и концентрации) с железом содержание оксида азота(II) в смеси составляет только 40% – меньше половины, а остальные 60% равномерно распределены между нитратом аммония, азотом, оксидом азота(I) и оксидом азота(IV) (рис. 8).
Следует отметить такой интересный и
жизненно важный факт, что со 100%-й азотной
кислотой ни железо, ни алюминий не реагируют
(следовательно, ее можно хранить и перевозить в
цистернах и других емкостях из этих металлов).
Дело в том, что эти металлы покрыты прочными
пленками оксидов, нерастворимых в чистой
кислоте. Для проявления кислотных свойств нужно,
чтобы кислота заметно диссоциировала, а для
этого в свою очередь требуется вода.
2. Реакции с неметаллами.
С кислородом и
озоном азотная кислота не реагирует.
3. Реакция с водой не происходит.
Вода
лишь способствует диссоциации кислоты.
4. Реакции с кислотами.
Азотная кислота
не реагирует с другими кислотами по типу реакций
обмена или соединения. Однако вполне способна
реагировать как сильный окислитель. В смеси
концентрированных азотной и соляной кислот
протекают обратимые реакции, суть которых можно
обобщить уравнением:
![]()
Образующийся атомарный хлор очень активен и
легко отбирает электроны у атомов металлов, а
имеющийся «под боком» хлорид-ион образует
устойчивые комплексные ионы с получающимися
ионами металлов. Все это позволяет перевести в
раствор даже золото. По той причине, что золото –
«царь металлов», смесь концентрированных
азотной и соляной кислот называют царской
водкой.
Концентрированная серная кислота как сильное
водоотнимающее средство способствует реакции
разложения азотной кислоты на оксид азота(IV) и
кислород.
5. Реакции с основаниями и с основными
оксидами
. Азотная кислота – одна из сильных
неорганических кислот и, естественно, со
щелочами реагирует. Реагирует она также и с
нерастворимыми гидроксидами, и с основными
оксидами. Этим реакциям способствует еще и то
обстоятельство, что все соли азотной кислоты
имеют хорошую растворимость в воде,
следовательно, продукты реакции не будут мешать
ее протеканию.
Физические свойства соединений NO, NO 2 и HNO 3 в цифрах
Оксид азота(II
) NO. Молярная масса 30 г/моль.
Температура плавления равна –164 °С,
температура кипения –154 °С. Плотность
газообразного NО при нормальных условиях (0 °С,
1 атм) 1,3402 г/л. Растворимость при атмосферном
давлении и 20 °С равна 4,7 мл газа NO на 100 г воды.
Оксид азота(IV
) NO 2 . Молярная масса 46
г/моль. Температура плавления –11 °С,
температура кипения 21 °С. Плотность
газообразного NO 2 при н. у. 1,491 г/л.
Растворимость – при условии, что этот оксид
сначала реагирует с водой на воздухе, а потом еще
и растворяется в получившейся азотной кислоте, –
можно считать неограниченной (вплоть до
образования 60%-й HNO 3).
Поскольку оксид азота(IV) активно димеризуется
(при 140 °С он целиком находится в виде мономера
NO 2 , однако при 40 °С мономера остается уже
около 30%, а при 20 °С он практически весь
переходит в димер N 2 O 4), то физические
свойства относятся скорее к димеру, чем к
мономеру. Именно этим можно объяснить достаточно
высокую температуру кипения (N 2 O 4
достаточно тяжелая молекула). О степени
димеризации можно судить по цвету: мономер
интенсивно окрашен, а димер бесцветен.
Азотная кислота
HNO 3 . Молярная масса 63
г/моль. Температура плавления –41,6 °С,
температура кипения 83 °С. Плотность жидкой
100%-й кислоты 1,513 г/см 3 . Растворимость
неограниченная, иными словами, кислота и вода
смешиваются в любых соотношениях. Стоит
отметить, что растворы азотной кислоты кипят при
температурах выше температур кипения чистых
воды и кислоты. При максимальной температуре
(122 °С) кипит 68,4%-й раствор, при этом процентный
состав раствора и пара одинаков.
Смеси веществ, для которых состав пара при
кипячении соответствует составу жидкости,
называют азеотропными или нераздельнокипящими.
(Слово «азеотроп» произошло от греч. – киплю, – изменение, – отрицательная приставка.) Для
более низких концентраций кислоты характерно
увеличение количества воды в паре по сравнению с
раствором, что приводит к концентрированию
раствора. При более высоких концентрациях,
наоборот, состав пара обогащен кислотой.
Химические свойства соединений азота (дополнение)
Как и всякие другие вещества, содержащие атом с
промежуточной степенью окисления, оксиды
азота(II) и (IV) в отличие от азотной кислоты могут
выступать и как окислители, и как восстановители,
в зависимости от партнера по реакции. Однако
многие из этих реакций «неактуальны» и
соответственно слабо изучены.
Из «актуальных» реакций стоит назвать реакцию
оксида азота(IV) с оксидом серы(IV) в присутствии
воды:
Актуальна эта реакция потому, что
присоединение кислорода к оксиду серы(IV)
протекает только при высоких температурах и в
присутствии катализатора, в то время как
присоединение кислорода к оксиду азота(II)
происходит при обычных условиях. Таким образом,
оксид азота(IV) как бы просто помогает оксиду серы
присоединить кислород. Протекает эта реакция при
обычных условиях (дополнительного давления в
смеси и нагревания не требуется).
Оксид азота(II
) тоже реагирует с оксидом
серы(IV), однако при совсем других условиях: или
при давлении в 500 атмосфер (!), тогда получаются
оксид серы(VI) и азот, или в водном растворе, тогда
получаются серная кислота и оксид азота(I).
Оксид азота(I
). Имеет слабый приятный запах и
сладковатый вкус. С кислородом, водой, растворами
кислот и щелочей не реагирует. Разлагается на
элементы при температуре выше 500 °С, иными
словами, достаточно устойчив.
Строение молекулы интересное: линейная молекула
О=N=N, в которой центральный атом азота
четырехвалентен. Он образует две двойные связи:
одну – с кислородом по типичной схеме создания
ковалентной связи (два электрона азота, два
электрона кислорода), другую – с атомом азота
(который два из своих трех неспаренных
электронов спаривает и образует за счет этого
пустую орбиталь), одна из связей – ковалентная,
вторая – донорно-акцепторная (рис. 9).
 |
Рис. 9. |
Оксид азота(III).
Состоит из NО и NO 2 ,
спаривших свои неспаренные электроны. Начинает
разлагаться на соответствующие газы уже при
плавлении (–101 °С).
Оксид азота(V).
Состоит из двух групп NO 2 ,
соединенных через кислород. Несколько более
устойчивое соединение, чем оксид азота(III),
начинает разлагаться при комнатной температуре.
Часть связей в нем, естественно,
донорно-акцепторные. И никаких «пятивалентных
азотов».
К химическим свойствам азотной кислоты следует
добавить, что она прекрасно реагирует с
неметаллами, которые может окислить. Так,
концентрированная азотная кислота реагирует и с
серой, и с фосфором, и с углем, образуя при этом
серную, фосфорную и угольную кислоты
соответственно.
Интересны и важны реакции азотной кислоты с
органическими веществами. Например, при
замещении трех атомов водорода в толуоле на
группы NO 2 образуется тринитротолуол (или
просто тол) – взрывчатое вещество.
Экологические свойства оксидов азота и азотной кислоты
Оксид азота(I)
относительно инертен, а
потому «экологически нейтрален». Однако на
человека он оказывает наркотическое действие,
начиная от просто веселья (за что он и был прозван
«веселящим газом») и заканчивая глубоким сном,
что нашло свое применение в медицине. Интересно,
что он безвреден, и для медицинского наркоза
применяют смесь оксида азота(I) с кислородом в
таком же соотношении, что и соотношение азота и
кислорода в воздухе. Наркотическое действие
снимается сразу после прекращения вдыхания
этого газа.
Два других устойчивых оксида азота легко
переходят один в другой, затем в кислоты, а затем
в анионы и. Таким образом, эти
вещества представляют собой естественные
минеральные удобрения, правда, если находятся в
естественных количествах. В «неестественных»
количествах эти газы редко попадают в атмосферу
в одиночестве. Как правило, образуется целый
«букет» ядовитых соединений, которые действуют
комплексно.
Например, всего один завод азотных удобрений
выбрасывает в воздух кроме оксидов азота,
азотной кислоты, аммиака и пыли от удобрений еще
и оксиды серы, соединения фтора, некоторые
органические соединения. Ученые выясняют
устойчивость различных трав, кустов и деревьев к
подобным «букетам». Уже известно, что, к
сожалению, ель и сосна неустойчивы и быстро
погибают, однако белая акация, канадский тополь,
ивы и некоторые другие растения могут
существовать в таких условиях, более того, они
способствуют удалению из воздуха этих веществ.
Сильное отравление оксидами азота можно
получить в основном при авариях на
соответствующих производствах. Ответная реакция
организма будет разной из-за различия в
свойствах этих газов. «Едкий» NО 2 в первую
очередь действует на слизистые оболочки
носоглотки, глаз, вызывает отек легких; NО, как
малорастворимое в воде и не едкое вещество,
проходит через легкие и попадает в кровь, вызывая
нарушения в центральной и периферийной нервных
системах. Оба оксида реагируют с гемоглобином
крови, хотя и по-разному, но с одинаковым
результатом – гемоглобин перестает переносить
кислород.
Экологические свойства азотной кислоты
складываются из двух «половинок». Как сильная
кислота, она разрушающе действует не только на
живые ткани (кожу человека, лист растения), но и на
почву, что достаточно актуально – кислотные
(из-за присутствия оксидов азота и серы) дожди,
увы, не редкость. При попадании кислоты на кожу
возникает химический ожог, который болезненнее и
заживает значительно дольше, чем термический.
Это были основные экологические свойства катиона
водорода.
Перейдем к изучению аниона
. При действии сильной кислоты на
передний план выдвигаются именно кислотные
свойства, поэтому свойства аниона лучше
рассмотреть на примере солей.
Взаимодействие нитрат-иона с фауной и флорой.
Дело в том, что нитрат-ион – неотъемлемая часть
круговорота азота в природе, он в ней всегда
присутствует. В обычных условиях и в
разбавленных растворах устойчив, слабо
проявляет окислительные свойства, не осаждает
катионы металлов, тем самым способствуя
транспортировке этих ионов с раствором в почве,
растениях и т. п.
Нитрат-ион становится ядовитым только в больших
количествах, нарушающих баланс других веществ.
Например, при избытке нитратов в растениях
уменьшается количество аскорбиновой кислоты.
(Стоит напомнить, что живой организм настолько
тонко организован, что любое вещество в больших
количествах нарушает равновесие и,
следовательно, становится ядовитым.)
Растения и бактерии используют нитраты для
построения белков и других необходимых
органических соединений. Для этого надо
перевести нитрат-ион в ион аммония. Эта реакция
катализируется ферментами, содержащими ионы
металлов (меди, железа, марганца и др.). Из-за
гораздо большей ядовитости аммиака и иона
аммония в растениях хорошо отработана и обратная
реакция перевода иона аммония в нитрат.
Животные не умеют строить все необходимые им
органические соединения из неорганических –
отсутствуют соответствующие ферменты. Однако
микроорганизмы, живущие в желудке и кишечнике,
этими ферментами обладают и могут переводить
нитрат-ион в нитрит-ион. Именно нитрит-ион и
действует как отравитель, переводя железо в
гемоглобине из Fe 2+ в Fe 3+ .
Соединение, содержащее Fe 3+ и называемое
метгемоглобином, слишком прочно связывает
кислород воздуха, следовательно, не может
отдавать его тканям. В результате организм
страдает от недостатка кислорода, при этом
происходят нарушения в работе мозга, сердца и
других органов.
Обычно нитрит-ион образуется не в желудке, а в
кишечнике и не успевает перейти в кровь и
произвести все эти разрушения. Поэтому
отравления нитратами достаточно редки.
Существует, правда, и другая опасность: в нашем
организме есть много веществ, в которых атомы
водорода аммиака замещены на органические
радикалы. Такие соединения называют аминами. При
реакции аминов с нитрит-ионами образуются
нитрозамины – канцерогенные вещества:
Они действуют на печень, способствуют образованию опухолей в легких и почках. Интересно, что активным замедлителем реакции образования нитрозаминов является давно нам знакомая аскорбиновая кислота.
О.Р.ВАЛЕДИНСКАЯ
(МГУ, Москва)
Оксидом азота называется инертный газ, который не обладает ароматическими качествами и цветом. Есть несколько соединений:
- Оксид (I) несолеобразующий. При условии высокой концентрации может спровоцировать возбуждение нервной системы. По-другому его называют веселящим газом. Свое применение оксид азота нашел как наркоз слабого действия в медицине;
- Монооксид азота – это газ, не обладающий цветом. Свойством оксида азота (II) является слабая степень растворимости в воде;
- Оксид (III) – это жидкость, обладающая темно-синим цветом. В нормальных условиях проявляет неустойчивость. При условии взаимодействия с водой способен образовывать азотистую кислоту;
- Оксид (IV) обладает газообразной формой, его окрас – бурый. В таком состоянии вещество тяжелее воздуха, поэтому способно легко сжиматься. Одним из свойств оксида азота является способность взаимодействовать с водой и щелочными растворами;
- Оксид (V) является веществом в кристаллической форме без цвета. Проявляет свойства сильного окислителя.
Оксид азота как пищевая добавка обладает свойствами антифламинга и глазирователя. Данное соединение также известно под наименованиями азотистый ангидрид, несолеобразующий оксид, диоксид азота, азотный ангидрид, триоксид диазота, монооксид азота, пентаоксид диазота, тетраоксид диазота, нитрозилазид, тринитрамид.
Применение оксида азота
Соединение в качестве добавки к продуктам питания практически не используется. Свое применение оксид азота нашел при упаковке продуктов, используется с целью приготовления аэрозольных масел, для взбивания сливок.
Благодаря своим особым свойствам соединение используется как газ-спрей в медицинских флаконах. Благодаря способности проявлять наркозный эффект оксид применяется в хирургической практике.
Оксид азота в организме
Как было установлено за последние годы, молекула оксида азота имеет широкий спектр биологического влияния. Данное действие можно поделить на защитное, регуляторное и вредное.
Оксид принимает участие в регуляции систем межклеточной и внутриклеточной сигнализации. Кроме того, соединение ответственно за эндотелиальное расслабление гладкой мускулатуры, принимает участие в процессах репродуктивной, иммунной, нервной системах. Показывает цитостатические и цитотоксические свойства.
Оксид клетками иммунной системы используется для уничтожения клеток злокачественных опухолей и бактерий. В случае нарушения метаболизма и биосинтеза оксида азота развивается бронхиальная астма, ишемическая болезнь сердца, первичная легочная гипертензия, инфаркт миокарда, невротическая депрессия, сахарный диабет, нейродегенеративные заболевания, импотенция, эссенциальная артериальная гипертензия.
Оксид азота в спорте
Наверное, многие слышали о продуктах, которые способны активизировать выработку оксида азота. Данные продукты в сфере пищевых добавок стали весьма популярными. Считается, что за счет усиления выработки оксида увеличивается приток крови к мышцам скелета, что положительно сказывается на организме атлета.
Согласно данным ученых Техасского университета, стадия, которая ограничивает скорость ткани аминокислот, отвечает за транспорт через межклеточную жидкость и кровь. Это означает, что усиление притока крови к мышцам скелета совместно с увеличением концентрации аминокислот обеспечивает более интенсивное поглощение мышечными клетками аминокислот.
Вред оксида азота
Несмотря ни на что, оксиды азота вредны и опасны для человеческого здоровья. Вследствие этого пищевая добавка относится к третьему классу опасности. Например, NO считается сильным ядом, который оказывает влияние на центральную нервную систему, может привести к поражению крови за счет связывания гемоглобина. NO2 также проявляет высокую токсичность, может спровоцировать раздражение дыхательных органов.
Популярные статьи Читать больше статей
 02.12.2013
02.12.2013
Все мы много ходим в течение дня. Даже если у нас малоподвижный образ жизни, мы все равно ходим – ведь у нас н...
605451 65 Подробнее
 10.10.2013
10.10.2013
Пятьдесят лет для представительниц прекрасного пола – это своеобразный рубеж, перешагнув который каждая вторая...
444883 117 Подробнее
 02.12.2013
02.12.2013
В наше время бег уже не вызывает массу восторженных отзывов, как это было лет тридцать назад. Тогда общество б...